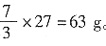银符考试题库B12
现在是:
试卷总分:100.0
您的得分:
考试时间为:
点击“开始答卷”进行答题
 价,变成N1,N2中的N为0价。所以化合价上升了
价,变成N1,N2中的N为0价。所以化合价上升了 ,总共有30个N上升,失去的电子说就是
,总共有30个N上升,失去的电子说就是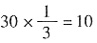 ,对于KNO3里面的N,由原来的+5价变成0价,得到5个电子,刚好有2个N在变化,得到电子数5×2=10。对于反应,化合价下降就是氧化物,化合价上升就是还原物。题目给出氧化物比还原物多1.75mol,采用差量法求出题目的反应产生刚好16个氮气,有30个N是失去电子升高的,变成15 N2,还有一个N2是由2个N下降得到电子变成的,差14个,所以差1.75mol时,N2的物质的量
,对于KNO3里面的N,由原来的+5价变成0价,得到5个电子,刚好有2个N在变化,得到电子数5×2=10。对于反应,化合价下降就是氧化物,化合价上升就是还原物。题目给出氧化物比还原物多1.75mol,采用差量法求出题目的反应产生刚好16个氮气,有30个N是失去电子升高的,变成15 N2,还有一个N2是由2个N下降得到电子变成的,差14个,所以差1.75mol时,N2的物质的量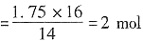 。A项,标准状况下2×22.4=44.8L,所以A错误。B项,对于KNO3是氧化剂,被还原。C项中,反应的NaN3物质的量
。A项,标准状况下2×22.4=44.8L,所以A错误。B项,对于KNO3是氧化剂,被还原。C项中,反应的NaN3物质的量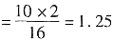 ,每mol含有三个N,所以等于3.75mol,同时NaN3也是还原剂,所以选项C错误。选项D中,转移的电子数计算氧化剂和还原剂得失电子一方就可以了,所以5×0.25=1.25mol,故选D。
,每mol含有三个N,所以等于3.75mol,同时NaN3也是还原剂,所以选项C错误。选项D中,转移的电子数计算氧化剂和还原剂得失电子一方就可以了,所以5×0.25=1.25mol,故选D。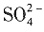 完全沉淀
完全沉淀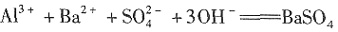 ↓+Al(OH)3↓
↓+Al(OH)3↓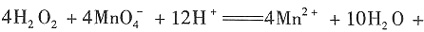 7O2↑
7O2↑ 恰好完全沉淀时,铝离子完全反应生成偏铝酸根离子,正确的离子方程式为:
恰好完全沉淀时,铝离子完全反应生成偏铝酸根离子,正确的离子方程式为: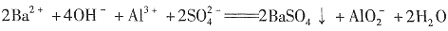 ,故A错误。B项中酸性高锰酸钾溶液中滴加H2O2溶液,该离子方程式中电子不守恒,正确的离子方程式为:
,故A错误。B项中酸性高锰酸钾溶液中滴加H2O2溶液,该离子方程式中电子不守恒,正确的离子方程式为: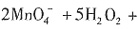 6H+====2Mn2++5O2↑+8H2O,故B错误;C项中,正确应该是:2Br-+Cl2====Br2+2Cl-。故选D。
6H+====2Mn2++5O2↑+8H2O,故B错误;C项中,正确应该是:2Br-+Cl2====Br2+2Cl-。故选D。
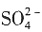
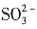 和
和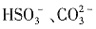 和
和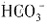 都能与HCl反应生成无色气体,故B错误;C项,溶液中含有银离子加入盐酸酸化的BaCl2溶液,有白色沉淀生成,该溶液中不一定含有
都能与HCl反应生成无色气体,故B错误;C项,溶液中含有银离子加入盐酸酸化的BaCl2溶液,有白色沉淀生成,该溶液中不一定含有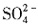 ,故C错误;D项,向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中加几滴新制的氯水,溶液变为红色,该溶液中一定含有Fe2+,故D正确;故选D。
,故C错误;D项,向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中加几滴新制的氯水,溶液变为红色,该溶液中一定含有Fe2+,故D正确;故选D。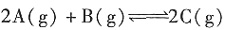 ;ΔH<0。5s后反应达到平衡状态,此时测定C的浓度为0.05mol/L。下列说法不正确的是______。
;ΔH<0。5s后反应达到平衡状态,此时测定C的浓度为0.05mol/L。下列说法不正确的是______。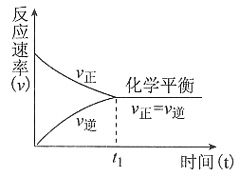
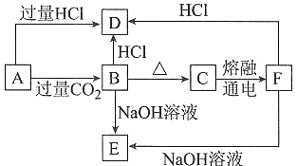


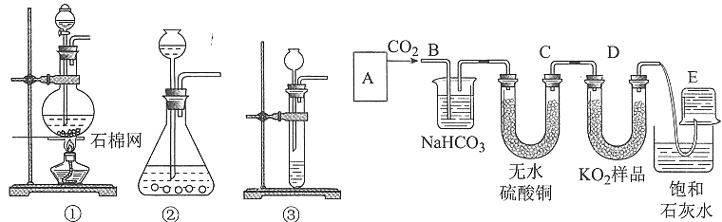
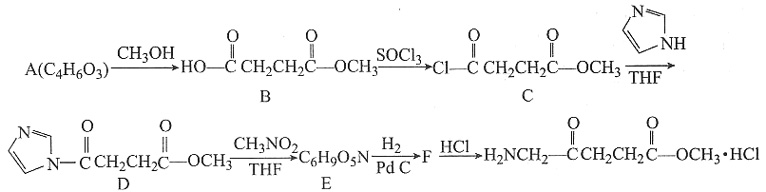
 ①主反应
①主反应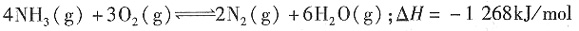 ②副反应
②副反应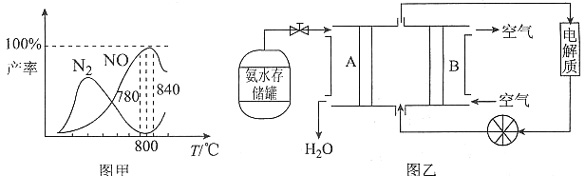
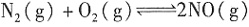 的反应热ΔH=______;由图甲可知工业上氨催化氧化生成NO时,反应温度最好控制在______。
的反应热ΔH=______;由图甲可知工业上氨催化氧化生成NO时,反应温度最好控制在______。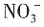 ,当控制溶液pH在10.7左右时,所得产物中还有氨气。若氨气和氮气的体积比为4:1,则除去62克的
,当控制溶液pH在10.7左右时,所得产物中还有氨气。若氨气和氮气的体积比为4:1,则除去62克的 ,消耗铝______克。
,消耗铝______克。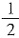 (①-②)可得反应③
(①-②)可得反应③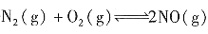 ,则反应③的反应热
,则反应③的反应热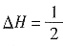 (-905 kJ/mol+1268 kJ/mol)=+181.5 kJ/mol;由图甲可知,温度在780~840℃时,NO生成率最大,所以工业上氨催化氧化生成NO时,反应温度最好控制在780~840℃。
(-905 kJ/mol+1268 kJ/mol)=+181.5 kJ/mol;由图甲可知,温度在780~840℃时,NO生成率最大,所以工业上氨催化氧化生成NO时,反应温度最好控制在780~840℃。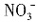 的物质的量为1mol,设生成NH3的物质的量为4xmol,则生成N2的物质的量为xmol,由题意可知:
的物质的量为1mol,设生成NH3的物质的量为4xmol,则生成N2的物质的量为xmol,由题意可知: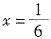
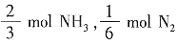 ,则共转移电子
,则共转移电子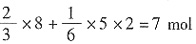
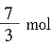 ,消耗Al的质量为
,消耗Al的质量为