一、选择题在每小题给出的四个选项中,只有一个选项是最符合题目要求的。4. 已知298K时,

则CH
4(g)+2O
2(g)=CO
2(g)+2H
2O(l)的

为______。
- A.211.0kJ·mol-1
- B.-890.3kJ·mol-1
- C.890.3kJ·mol-1
- D.-622.2kJ·mol-1
A B C D
B
[考点] 本题考查反应的标准摩尔焓变的计算。
[解析] 由反应式(1)+2×反应式(2)+反应式(3)可得总反应式,则:

8. 已知

。298K时,反应2Fe
3++Sn
2+=2Fe
2++Sn
4+的

为______。
A.

B.

C.

D.

A B C D
B
[考点] 本题考查氧化还原反应的标准平衡常数的计算。
[解析]

13. 向0.10mol·L
-1的下列溶液中滴加甲基红指示剂,溶液颜色为橙色的是______。
- A.HCl
- B.Na2C2O4
- C.NH4Cl
- D.NaHCO3
A B C D
C
[考点] 本题考查酸碱质子理论、溶液的酸碱性、指示剂的变色范围及颜色变化等。
[解析] 甲基红的实际变色范围为4.4~6.2,其酸式色为红色,碱式色为黄色,中间过渡色为橙色。HCl为强酸,溶液浓度为0.10mol·L
-1时,其pH=1.00,此时溶液呈红色。

均为弱碱,其溶液pH>7.00,故溶液均呈黄色。

为弱酸,此浓度下,其溶液pH约为5.13,故溶液呈橙色。
19. 可用AgNO
3/CH
3CH
2OH夏别的一组化合物是______。
A.

B.

C.

D.

A B C D
D
[解析] A、B、C各组都是相同类型的卤代烃,而D组前者为乙烯型卤代物,不反应,后者为烯丙型卤代物,反应速度快。
二、填空题1. 用0.1000mol·L
-1NaOH标准溶液滴定同浓度的

溶液,滴定突跃范围的pH=7.74~9.70。若浓度改为0.01000mol·L
-1,滴定突跃范围的pH=7.74~______
8.70
[考点] 本题考查滴定突跃范围的影响因素。
[解析] 强碱滴定强酸时,仅浓度为主要影响因素;强碱滴定弱酸时,主要影响因素为浓度和弱酸的
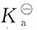
。终点误差为-0.1%时,溶液中弱酸及其共轭碱的浓度比为1:999,

;终点误差为+0.1%时,溶液pH取决于溶液中过量的NaOH的浓度,即强碱浓度降为原来的1/10时,pH约降低一个单位。
2. NaNO
3、NaSO
4、MgCl
2和AlCl
3对AgCl溶胶的聚沉值(mmol·L
-1)分别为300、295、25和0.5,则聚沉能力最大的电解质是______。
AlCl3
[考点] 本题考查溶胶的聚沉。
[解析] 由于电解质含有与胶粒所带电荷相反的离子,因此加入电解质可造成溶胶聚沉,且离子电荷越高,对溶胶的聚沉作用就越大,其聚沉值越小。
3. 298K时,在C(石墨)、O
2(g)、H
2(g)和Br
2(g)中,

不为零的是______。
Br2(g)
[考点] 本题考查物质的标准摩尔生成焓

的定义,即在温度T,由参考状态的元素单质生成1mol该物质时的标准摩尔焓变。
[解析] 参考状态单质一般是指每个元素在所讨论的温度和压力下最稳定的状态。溴单质在常温下是液态,故Br
2(g)的

的数值不为零。
4. 某有色溶液用1cm比色皿测得吸光度A=0.300。此溶液稀释一倍后,在相同波长下测定,欲使溶液吸光度A=0.450,应使用______cm的比色皿。
3
[考点] 本题考查分光光度法中的光吸收定律(朗伯-比尔定律)。
[解析] 吸光度A和浓度c及比色皿厚度b之间的关系:A=εbc,测试条件不变、测定波长不变,则ε不变,据此可计算出A=0.450时的b。
5. Cu的基态价电子构型为3d
104s
1,其4s电子的四个量子数取值为______。
[考点] 本题考查量子力学中,描述原子核外电子运动状态的4个量子数及其取值规则。
[解析] 其中,主量子数n表示电子层数;角量子数l表示同一电子层中不同状态的亚层,可取0、1、2、…、n-1;磁量子数m与原子轨道的空间伸展方向有关,可取0、±1、±2、…、±l;自旋量子数m
s与电子自旋运动状态有关,可取

。
6. 氢氧化二氨合银(I)的化学式为______。
[Ag(NH3)2]OH
[考点] 本题考查配合物的命名和书写。
7. 反应2NO
2(g)+F
2(g)=2NO
2F(g)的速率方程为v=kc(NO
2)·c(F
2),其反应级数为______。
2
[考点] 本题考查化学反应速率方程式和反应级数。
[解析] 总反应级数等于速率方程式中各反应物的分级数之和。
8. 测定pH时,常用的指示电极为______。
玻璃电极
[考点] 本题考查电势分析法中原电池的组成。
[解析] 构成原电池的两个电极中,指示电极的电极电势能够响应被测离子活度(或浓度)或其变化,参比电极的电极电势恒定,不受试液组成变化的影响。测定pH时,常用的指示电极为基于H+选择性电极的玻璃电极。
9. 溶液中下列离子性质的判断,正确的是______。(填序号)
①碱性:

②氧化性:

③稳定性:[Cu(CN)
4]
3->[Cu(NH
3)
4]
2+>[CuY]
2-
②
[考点] 本题考查物质的酸碱性、氧化还原性和配合物的稳定性。
[解析] 选项①中,三种碱所对应的共轭酸的酸性强弱顺序是:

,因此这三种碱的碱性顺序应相反。选项③中,Y为多基配体,[CuY]
2-为螯合物,比简单配合物更稳定;[Cu(CN)
4]
3-和[Cu(NH
3)
4]
2+虽然都是外轨型配合物,但是CN
-和中心离子结合更强,所以[Cu(CN)
4]
3-比[Cu(NH
3)
4]
2+更稳定。
10. 配离子[AlF
6]
3-的空间构型为______。
正八面体
[考点] 本题考查配位化合物的价键理论。
[解析] Al3-作为中心离子,其核外电子结构为2s22p6,内层没有d电子,只能形成外轨型配合物;而F-作为配体,元素电负性大,其孤对电子只能进入中心原子的外层轨道,倾向于生成外轨型配合物。故[AlF6]6-中Al3+为sp3d2杂化,分子构型为正八面体。
11. 反应

的产物有乙酸、乙醇和______。(填名称)
12.

的系统命名是______。
13. 调节谷氨酸水溶液至其等电点,应向该溶液中加______。(填“碱”或“酸”)
14. 5-硝基-2-萘酚的结构式为______。
15. 结构

对应的Newman投影式为______。
16. 制备乙酰苯胺的原料分别是乙酸酐和______。(填名称)
17. 化合物

在光照下进行溴代反应,最容易被取代的是______号碳上的氢原子。(填序号)
18. 化合物

在酸性条件下脱水的主要产物是______。(填结构式)
19. 反-1,2-二苯乙烯的结构式为______。
20. 完成反应式(写出主产物):

______。
三、计算、分析与合成题共50分。1. 向血红色的Fe(NCS)
3溶液中滴加过量NH
4F溶液会出现什么现象?说明理由。
已知

。
红色变无色。
因为会发生反应Fe(NCS)3+6F-=[FeF6]3-+3SCN-
红色的Fe(NCS)3能转化为无色的[FeF6]3-。
2. 溶液中含有相同浓度的Cu
2+、Ce
4+和Ag
+,欲使Ce
4+和Ag
+还原为Ce
3+和Ag,而Cu
2+不被还原,在还原剂H
2O
2和SnCl
2中应选择哪一个?为什么?

选择H
2O。

,说明在溶液中Sn
2+的还原性较强,可将Cu
2+、Ce
4+和Ag
+还原。

,所以在溶液中H
2O
2能还原Ce
4+和Ag
+,不能还原Cu
2+。
3. 向0.050mol·L
-1K
2CrO
4溶液中滴加AgNO
3溶液,计算:
(1)开始生成沉淀时,溶液中c(Ag
+);
(2)溶液中c(Ag
+)=1.0×10
-5mol·L
-1时,已沉淀的

的百分数。
已知

。
4. 若在常压下100℃沸水中煮熟鸡蛋需要3min,而在大气压较低的高原地区,在90℃沸水中煮熟鸡蛋需要6min。假设鸡蛋煮熟所需时间和蛋白质变性的速率成反比,计算煮熟鸡蛋过程中反应(即蛋白质变性)的活化能。
根据题意,鸡蛋煮熟所需时间和蛋白质变性的速率成反比。

E
a=7.8×10
4J·mol
-1=78kJ·mol
-1
5. 用重铬酸钾法测定含铁约60%的某铁矿样品。现用0.05000mol·L
-1K
2Cr
2O
7标准溶液测定,计算铁矿样品的称量范围。已知M(Fe)=55.85g·mol
-1。
离子反应式:


滴定体积20mL~30mL:
m(Fe)=6×0.05000×(20~30)×10
-3×55.85=0.34~0.50g
样品称量范围:

6. 化合物A(C
9H
10)能使溴的四氯化碳溶液褪色,催化加氢生成B(C
9H
12);B用酸性高锰酸钾氧化生成C(C
8H
6O
4);C加热失水生成邻苯二甲酸酐。写出A、B、C的结构式。
C加热失水生成邻苯二甲酸酐,故C为邻苯二甲酸(符合C
8H
6O
4)。同时可以推导出B为苯环邻位二取代结构,A催化加氢生成B,故A也是苯环邻位二取代结构。A化合物C
9H
10不饱和度为5,除苯环外,还剩余3个碳,1个不饱和度(溴的四氯化碳溶液褪色为双键);因为是邻位二取代,只有邻甲基苯乙烯符合。所以A、B、C的结构式为:

7.

此组3个化合物中苯乙醛可以与Fehling试剂反应生成砖红色沉淀,其余二者不反应。2,4-二硝基苯肼可以与剩余的苯基丙酮生成沉淀,醇不反应。用流程图表示的鉴别过程如下:

8.

此组3个化合物分别是氨基酸、羟基酸和卤代酸,水合茚三酮与氨基酸反应呈蓝紫色,其余二者不反应。卤代酸相当于卤代物,与AgNO
3的醇溶液发生反应产生卤化银沉淀,羟基酸不反应。用流程图表示的鉴别过程如下:

9. 由

和2个碳原子的有机试剂制备

;
目标产物为羧酸酯,酸部分比原料环己烯多一个碳,可以从环己烯与溴化氢加成生成溴代环己烷,再与NaCN反应,进而水解得到;醇部分可以使用乙醇;然后环己烷甲酸与乙醇在酸催化下酯化得到产物。制备过程如下:

10. 由

和3个碳原子的有机试剂制备

。
目标产物为仲醇,可以通过酮的选择性还原得到(只还原羰基,不还原硝基)。合成的策略是原料苯先进行付-克酰基化反应得到苯基丙酮,而后再硝化生成间位定位的硝基(注意:先硝化后酰基化行不通)。制备过程如下:


 为______。
为______。
 的标准平衡常数
的标准平衡常数 ,在相同温度下,反应A2B=2A+B的
,在相同温度下,反应A2B=2A+B的 为______。
为______。 。298K时,反应2Fe3++Sn2+=2Fe2++Sn4+的
。298K时,反应2Fe3++Sn2+=2Fe2++Sn4+的 为______。
为______。





 均为弱碱,其溶液pH>7.00,故溶液均呈黄色。
均为弱碱,其溶液pH>7.00,故溶液均呈黄色。 为弱酸,此浓度下,其溶液pH约为5.13,故溶液呈橙色。
为弱酸,此浓度下,其溶液pH约为5.13,故溶液呈橙色。 进行亲电取代反应,活性从大到小的顺序是______。
进行亲电取代反应,活性从大到小的顺序是______。























 ,下列描述符合该结构的是______。
,下列描述符合该结构的是______。


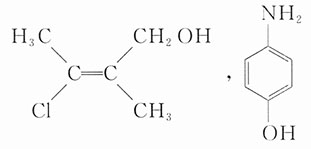




 可能的产物有______。
可能的产物有______。 溶液,滴定突跃范围的pH=7.74~9.70。若浓度改为0.01000mol·L-1,滴定突跃范围的pH=7.74~______
溶液,滴定突跃范围的pH=7.74~9.70。若浓度改为0.01000mol·L-1,滴定突跃范围的pH=7.74~______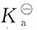 。终点误差为-0.1%时,溶液中弱酸及其共轭碱的浓度比为1:999,
。终点误差为-0.1%时,溶液中弱酸及其共轭碱的浓度比为1:999, ;终点误差为+0.1%时,溶液pH取决于溶液中过量的NaOH的浓度,即强碱浓度降为原来的1/10时,pH约降低一个单位。
;终点误差为+0.1%时,溶液pH取决于溶液中过量的NaOH的浓度,即强碱浓度降为原来的1/10时,pH约降低一个单位。 不为零的是______。
不为零的是______。 的定义,即在温度T,由参考状态的元素单质生成1mol该物质时的标准摩尔焓变。
的定义,即在温度T,由参考状态的元素单质生成1mol该物质时的标准摩尔焓变。 的数值不为零。
的数值不为零。
 。
。

 ,因此这三种碱的碱性顺序应相反。选项③中,Y为多基配体,[CuY]2-为螯合物,比简单配合物更稳定;[Cu(CN)4]3-和[Cu(NH3)4]2+虽然都是外轨型配合物,但是CN-和中心离子结合更强,所以[Cu(CN)4]3-比[Cu(NH3)4]2+更稳定。
,因此这三种碱的碱性顺序应相反。选项③中,Y为多基配体,[CuY]2-为螯合物,比简单配合物更稳定;[Cu(CN)4]3-和[Cu(NH3)4]2+虽然都是外轨型配合物,但是CN-和中心离子结合更强,所以[Cu(CN)4]3-比[Cu(NH3)4]2+更稳定。 的产物有乙酸、乙醇和______。(填名称)
的产物有乙酸、乙醇和______。(填名称) 的系统命名是______。
的系统命名是______。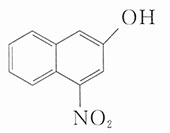
 对应的Newman投影式为______。
对应的Newman投影式为______。
 在光照下进行溴代反应,最容易被取代的是______号碳上的氢原子。(填序号)
在光照下进行溴代反应,最容易被取代的是______号碳上的氢原子。(填序号) 在酸性条件下脱水的主要产物是______。(填结构式)
在酸性条件下脱水的主要产物是______。(填结构式)

 ______。
______。
 。
。
 ,说明在溶液中Sn2+的还原性较强,可将Cu2+、Ce4+和Ag+还原。
,说明在溶液中Sn2+的还原性较强,可将Cu2+、Ce4+和Ag+还原。 ,所以在溶液中H2O2能还原Ce4+和Ag+,不能还原Cu2+。
,所以在溶液中H2O2能还原Ce4+和Ag+,不能还原Cu2+。 的百分数。
的百分数。 。
。
 百分数为:
百分数为:









 和2个碳原子的有机试剂制备
和2个碳原子的有机试剂制备 ;
;
 和3个碳原子的有机试剂制备
和3个碳原子的有机试剂制备 。
。
