一、知识概念题
1.单选题1. 用浓度为98%的浓硫酸和40%的稀硫酸配制100kg80%的硫酸,则所需要的原料酸______。
- A.浓硫酸用量多
- B.稀硫酸用量多
- C.浓硫酸、稀硫酸各一半
- D.无法配制
A B C D
A
[解析] 解:设98%的H
2SO
4需要量为x kg,40%的H
2SO
4需要量为y kg。
对H
2SO
4进行衡算:
0.98x+0.4y=0.8(x+y)
0.98x-0.8x=0.8y-0.4y
0.18x=0.4y

x>y。即浓度为98%的硫酸用量多。
7. 假设反应器内只发生乙烯和苯作用生成乙苯的反应,乙烯的转化率为100%。反应为:
C
2H
4+7C
6H
6→C
2H
5C
6H
5+6C
6H
6 由物化手册查得这三种组分的标准生成热
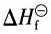
分别为

则该反应的反应热ΔH
r为______。
- A.-105.34kJ/mol
- B.105.34kJ/mol
- C.164.86kJ/mol
- D.-164.86kJ/mol
A B C D
A
[解析] 解:本题是利用参加反应的各物质的标准生成热计算化学反应热。

8. 反应2HNO
3→N
2O
5+H
2O,N
2O
5生成量计算公式为______。(M
HNO3和M
N2O5分别代表HNO
3和N
2O
5的相对分子质量)
A.

B.

C.

D.
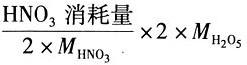
A B C D
9. 气体混合物的组成和100℃的定压摩尔热容C。值如下表所示。混合物组成与100℃定压摩尔热容C
p值
| 组分 | 乙烯 | 丙烯 | ∑ |
| 摩尔百分数/% | 30 | 70 | 100 |
| Cp,m/(kJ/(kmol·K)) | 56.484 | 79.83 | — |
则混合气体的定压摩尔热容为______kJ/(kmol·K)。
- A.68.16
- B.79.83
- C.72.83
- D.56.48
A B C D
C
[解析] 解:对于理想状态下的混合气体,热容可以按以下公式计算:

N
1=0.3(摩尔分数),

N
2=0.7(摩尔分数),


14. 以生产1t氨计算,含惰性气体0.2%(体积百分数,下同)的新鲜气消耗量为2800m
3,循环气中惰性气体的含量不超过3%,氨冷凝的温度为20℃,氨冷凝的总压力为30.0MPa。则排放气体量为______。
不同温度下的溶解度系数:

- A.111m3/t液氨
- B.186.7m3/t液氨
- C.75.8m3/t液氨
- D.101m3/t液氨
A B C D
A
[解析] 解:新鲜气中惰性气体量为
2800×0.002=5.6m
3 根据题意,20℃下,氨液溶解气体0.256m
3/t氨(常压下)。
30.0MPa、20℃下,惰性气体含量为
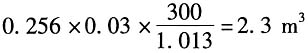
1t氨排放的气体量(体积)为

17. 有关温度、压力对物质焓值的影响的论述,不正确的是______。
A.温度对焓的影响主要通过

来计算
B.压力对焓的影响通过

来计算
C.在绝大多数情况下ΔH
p比ΔH
T重要得多
D.理想气体的焓随压力而变
A B C D
19. 关于气相化学平衡计算的论述,不正确的是______。
A.

,一般可认为
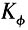
与组成无关
B.K
f=K
yp
vi只适用于理想气体间的反应
C.K
f只是温度的函数
D.

只适用于平衡混合物是理想混合物的情况
A B C D
2.多选题3. 用废热锅炉回收高温气体的热量。高温气体走管内,管外送入30℃、压力为1.274MPa的软水,产生1.274MPa的饱和蒸汽,高温气体在废热锅炉内被冷却降温,放出1.49×10
7kJ/h的热量,热损失为气体所放出热的3%,产生的蒸汽量不正确的有______。
已知:30℃、1.274MPa的饱和水的焓H
1=125.484kJ/kg,1.274MPa的饱和蒸汽的焓H
2=2784.7kJ/kg。
- A.5603kg/h
- B.5434kg/h
- C.56031kg/h
- D.54339kg/h
A B C D
ACD
[解析] 解:软水汽化取出的热量为
Q=1.49×10
7×(1-0.03)=1.445×10
7kJ/h
产生的蒸气量为

二、案例分析题1. 在年产1500t的乙苯脱氢制取苯乙烯装置中,加入的水蒸气量为2.6kg水蒸气/kh苯乙烯,在650℃下乙苯的转化率为44.4%,苯乙烯的收率为40%,其余副产物为苯3%、甲苯5%、焦碳2%。装置年工作日为300天,已知原料乙苯的纯度为98%(wt),其余为甲苯。则反应后产生的气体总量为______。
反应方程式为


- A.8.52kg
- B.8.35kg
- C.8.53kg
- D.7.676kg
A B C D
C
[解析] 解:(1)每小时苯乙烯的产量为
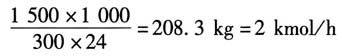
每小时需要的乙苯量为
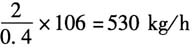
每小时转化的乙苯量为
530×0.444=235.32kg/h=2.22kmol/h
未反应的乙苯量为
530-235.32=294.68kg/h
每小时需要的水蒸气量为
530×2.6=1378kg
每小时需要原料乙苯的量为

,其中甲苯的量为10.8kg。
(2)产物中各组分的量
苯乙烯:208.3kg

苯:2.22×0.03×78=5.19kg
焦炭:2.22×0.02×7×12=3.73kg
乙苯:294.68kg
乙烯(气):2.22×0.03×28=1.86kg
甲烷(气):(2.22×0.05+2.22×0.02)×16=2.49kg
氢(气):(2+2.22×0.02×3-2.22×0.02)×2=4.178kg
气体总量:1.86+2.49+4.178=8.53kg。
2. 苯发生氯化反应得到的最终混合物组成为氯化苯39%(wt,下同)、二氯化苯1%、苯60%。
已知各物质的生成热

分别为苯49.061kJ/mol、氯化苯-52.17kJ/mol、二氯化苯-53.05kJ/mol、氯化氢-92.36kJ/mol。
1t苯在反应过程中所释放的热量接近______。
- A.788kJ
- B.78369kJ
- C.788700kJ
- D.89418.68kJ
A B C D
C
[解析] 解:化学反应方程:
C
6H
6+Cl
2→C
6H
5Cl+HCl
C
6H
6+2Cl
2→C
6H
4Cl
2+2HCl
相对分子质量:C
6H
678,C
6H
5Cl 112.5,C
6H
4Cl
2 147。
基准:物料计算为100kg反应物,热量计算为1000kg苯。
(1)物料衡算
在100kg反应后的混合物中,含C
6H
6 60kg、C
6H
5Cl 39kg、C
6H
4Cl
2 1kg。
生产氯化苯消耗的苯量为

生产二氯化苯消耗的苯量为

未反应的苯量为
W
0=60kg
因此,生成100kg混合物,所消耗的苯总量为
W=W
0+W
1+W
2=60+27.04+0.53=87.57kg
1t苯可得反应混合物
1000/0.8757=1142kg
其中,氯化苯为1142×0.39=445.4kg,二氯化苯为1142×0.01=11.4kg,苯为1142×0.6=685.2kg。
(2)热量衡算
反应的热效应

反应的热效应
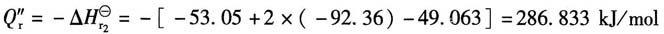
所以1t苯氯化所释放的热量为
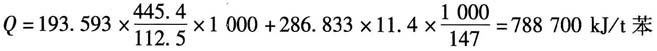
3. 乙烯在银催化剂上用过量空气部分氧化制取环氧乙烷,化学反应方程式为:主反应

,副反应

。反应器进口混合气体的流量为45000m
3·h
-1(标准状态下),原料组成为C
2H
4 3.5%(mol%,下同),N
2 82.0%,O
2 14.5%。乙烯的转化率为32%,反应的选择性为69%,则反应器出口气体的流量为多少kg·h
-1?若已知主反应的反应热为
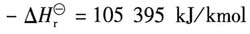
乙烯,该过程主反应的反应热是______。
- A.57415.2,2.37×106kJ
- B.57415.2,1.64×106kJ
- C.57415.2,5.11×106kJ
- D.50234,1.64×106kJ
A B C D
B
[解析] 解:(1)物料计算。以1小时的气体流量为基准。
进口混合气体的平均分子量

进气质量为
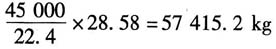
根据质量守恒,反应器出口气体质量同为57415.2kg。
(2)化学反应热计算。
进口处乙烯的摩尔数为

参与主反应的乙烯量为
70.3×0.32×0.69=15.52kmol
主反应的反应热为
Q=15.52×1.05395×10
5=1.64×10
6kJ
4. 正庚烷和乙苯的混合物中含正庚烷42%(mol%,下同)、乙苯58%,在101.3kPa下精馏。进料为112.5℃的饱和液体,塔顶产品和塔底产品也均为饱和液体,温度分别为99℃和135℃,物料衡算列于下表。
| 编 号 | 组成 | 进料/kmol·h-1
N1 | 塔顶产品/kmol·h-1
N2 | 塔底产品/kmol·h-1
N3 |
1
2
合计 | 正庚烷
乙 苯 | 20.30 x1
28.00 x2
48.30 | 20.00 x21
0.63 x22
20.63
| 0.30 x31
27.37 x32
27.67 |
塔顶冷凝器取走热量2.298×10
6kJ·h
-1。再沸器的热负荷近似为______。
已知:正庚烷和乙苯的平均定压摩尔热容分别为
C
p1=217.3kJ/(kmol·K),C
p2=181.7kJ/(kmol·K)
- A.2.35×106kJ/h
- B.5.34×104kJ/h
- C.2.35×105kJ/h
- D.2.35×107kJ/h
A B C D
A
[解析] 解:取计算基准为1h的量,基准温度为0℃。
设进塔物料带入的热量为Q1,塔底和塔顶产品带出的热量分别为QW和QP,冷凝器取走的热量为QD,再沸器传入的热量为Q2。
热量平衡方程:Q1+Q2=QP+QW+QD。
根据题意和已知条件:
Q1=20.30×217.3×112.5+28.00×181.7×112.5
=1.0686×106kJ
QP=20.00×217.3×99+0.63×181.7×99
=0.4416×106kJ
QW=0.30×217.3×135+27.37×181.7×135
=0.6802×106kJ
QD=2.298×106kJ
Q2=QP+QW+QD-Q1
=(0.4416+0.6802+2.298-1.0686)×106
=2.3512×106kJ
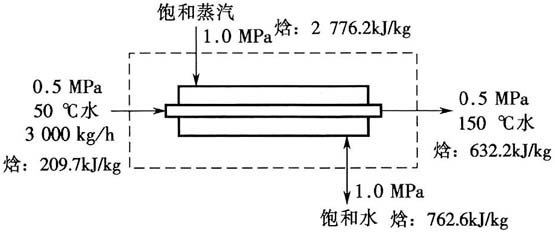
5. 利用蒸汽在套管换热器中预热软水(如下图所示)。软水量为3000kg/h,压力为0.5MPa,水温由50℃升高到150℃。采用1.0MPa的饱和蒸汽,冷凝后变为饱和水,则所需蒸汽流量最接近______。
- A.629.5kg/h
- B.14274.8kg/h
- C.705.5kg/h
- D.14264.4kg/h
A B C D
A
[解析] 解:假定换热器绝热良好,热损失可忽略。系统动能、势能无变化,无外部做功。则
F
汽(H
1.0MPa,汽-H
1.0MPa,水)=F
水(H
0.5MPa,150℃-H
0.5MPa,50℃)
查得1.0MPa下饱和蒸汽与饱和水的焓分别为H
1.0MPa,汽=2776.2kJ/kg,H
1.0MPa,水=762.6kJ/kg;
0.5MPa下,150℃水的焓H
0.5MPa,150℃=632.2kJ/kg,50℃水的焓H
0.5MPa,50℃=209.7kJ/kg。
F
水=3000kg/h

8. 用清水吸收含二氧化硫5%(体积百分数)的混合气体,混合气流量为2000m
3/h(STP),吸收率为80%。吸收用水水温为20℃,操作压力为0.1MPa(绝压)。则吸收时水的最小用量为______。
已知:二氧化硫在20℃时的溶解度数据如下:

- A.34.8t
- B.32.4t
- C.30.9t
- D.35.6t
A B C D
C
[解析] 解:令y
1、y
2为吸收前、后二氧化硫在气体中的摩尔分数,x、x
2为吸收前、后SO
2在水中的摩尔分数,L为水用量。
y
1=5/95=0.0526kmol SO
2/kmol惰气
y
2=0.0526×(1-0.8)=0.0105kmol SO
2/kmol惰气
液面压力下SO
2溶解度的计算:分压为760×0.05=38mmHg相对应的溶解度为

惰性气体的摩尔数为

v(y
1-y
2)=L×0.00194
L=1714kmol=30.85t

 ,A为关键组分,P为目的产物;FAO为进料A的摩尔流量,且进口物料中不含P,FP为反应器出口处P的摩尔流量;则P的收率正确的计算公式是______。
,A为关键组分,P为目的产物;FAO为进料A的摩尔流量,且进口物料中不含P,FP为反应器出口处P的摩尔流量;则P的收率正确的计算公式是______。




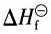 分别为
分别为




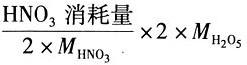




 计算:
计算:

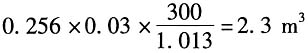

 来计算
来计算 来计算
来计算
 ,一般可认为
,一般可认为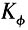 与组成无关
与组成无关 只适用于平衡混合物是理想混合物的情况
只适用于平衡混合物是理想混合物的情况







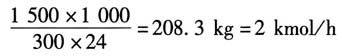
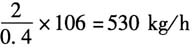
 ,其中甲苯的量为10.8kg。
,其中甲苯的量为10.8kg。
 分别为苯49.061kJ/mol、氯化苯-52.17kJ/mol、二氯化苯-53.05kJ/mol、氯化氢-92.36kJ/mol。
分别为苯49.061kJ/mol、氯化苯-52.17kJ/mol、二氯化苯-53.05kJ/mol、氯化氢-92.36kJ/mol。


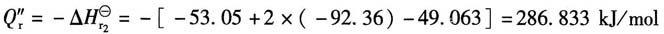
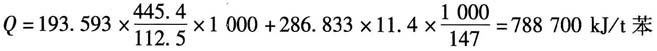
 ,副反应
,副反应 。反应器进口混合气体的流量为45000m3·h-1(标准状态下),原料组成为C2H4 3.5%(mol%,下同),N2 82.0%,O2 14.5%。乙烯的转化率为32%,反应的选择性为69%,则反应器出口气体的流量为多少kg·h-1?若已知主反应的反应热为
。反应器进口混合气体的流量为45000m3·h-1(标准状态下),原料组成为C2H4 3.5%(mol%,下同),N2 82.0%,O2 14.5%。乙烯的转化率为32%,反应的选择性为69%,则反应器出口气体的流量为多少kg·h-1?若已知主反应的反应热为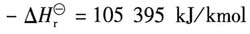 乙烯,该过程主反应的反应热是______。
乙烯,该过程主反应的反应热是______。
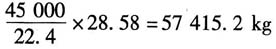


 。
。 。
。


