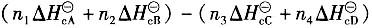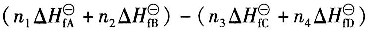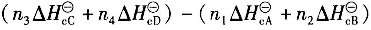一、单选题2. 硫酸铝可由含Al
2O
3的混合物与H
2SO
4反应制得。反应方程如下:

Al
2O
3的混合物中含杂质44.6%(质量分数,下同),原料硫酸为80%,的H
2SO
4,其余为H
2O。用1100kg Al
2O
3、2510kg80%的H
2SO
4,则过量的一种原料的转化率是______。假定Al
2O
3,全部转化。
- A.70.42%
- B.87.4%
- C.69.96%
- D.29.13%
A B C D
B
[解析] 解:按反应方程和已知条件计算如下。
Al
2O
3相对分子质量为102,Al
2(SO
4)
3相对分子质量为342,H
2SO
4相对分子质量为98。
加入硫酸(80%)量为2510kg,含纯H
2SO
4量为
2510×0.8=2008kg=20.49kmol
加入原料Al
2O
3混合物1100kg,含纯Al
2O
3量为
1100×0.554=609.4kg=5.97kmol
参加反应的H
2SO
4量应为5.97×3=17.91kmol。
在反应系统中H
2SO
4过量,过量20.49-17.91=2.58kmol
H
2SO
4转化率为
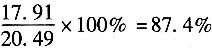
。
3. 在利用硫化矿提炼锌时,硫酸是副产物。该矿中含ZnS65%(质量分数,下同),其他35%为惰性物质。生产过程如反应方程所示,最后可以得到98%的硫酸,硫的回收率为99%,每天处理硫化矿186t。
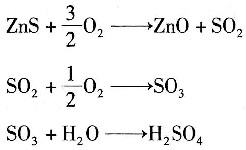
则每天需要水的量是______。
- A.24.67t
- B.22.2t
- C.2.47t
- D.24.92t
A B C D
A
[解析] 解:根据反应方程可知,当1mol的ZnS反应时,就可以产生1mol的H
2SO
4,即可以产生98%的H
2SO
4100g。
根据题意硫的回收率为99%,再进行计算。
(1)每天处理186t矿石,则内含ZnS量为
186×1000×0.65=120900kg
实际反应能得到硫酸的ZnS量为120900×0.99=119691kg
119691kg ZnS为1233.9kmol,即可生成1233.9kmol H
2SO
4,质量为120922.2kg,可以得到
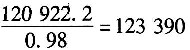
kg 98%的硫酸。
(2)用水量计算:吸收SO
3形成H
2SO
4的用水量为1233.9×18=22.2t,形成98%的H
2SO
4的用水量为123390-120922.2=2.47t。
每天消耗水量为22.2+2.47=24.67t。
4. 将78%(质量分数,下同)的H
2SO
4加到水中配制成25%的H
2SO
4,配制1000kg25%的H
2SO
4放出的热量为______。
已知:78%的H
2SO
4积分溶解热为37656J/mol H
2SO
4,25%的H
2SO
4积分溶解热为69454.4J/mol H
2SO
4。
- A.8.1×107kJ
- B.8.1×104kJ
- C.8.1×102kJ
- D.81kJ
A B C D
B
[解析] 解:1000kg25%的H
2SO
4含溶质H
2SO
4 250kg,则
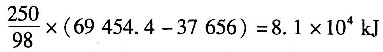
13. 在含苯38%(质量分数,下同)和甲苯62%的混合液连续精馏过程中,要求馏出物中能回收原料中97%的苯,釜残液中含苯不高于2%。进料流量为20000kg/h,则塔顶苯的摩尔分数近似比为______。
A B C D
B
[解析] 解:以进塔苯和甲苯的混合物每小时20000kg为基准。
设进料量为F,塔顶液量为D,塔釜液量为W。以下标B代表苯。
进料中苯的摩尔分数
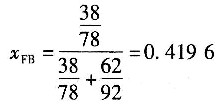
釜残液中苯的摩尔分数
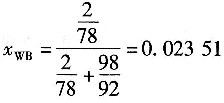
进料液的平均分子质量
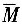
=0.4196×78+(1-0.4196)×92=86.13
进塔物料的摩尔流量
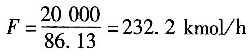
依题意,馏出液中能回收原料中97%的苯,所以

作全塔苯的质量衡算:
Fx
FB=Dx
DB+Wx
WB 作全塔总质量衡算:
F=W+D
将已知数据代入上述质量衡算方程得
232.2×0.4196=94.51+0.02351W (A)
232.2=W+D (B)
由式(A)得W=124.25kmol/h,由式(B)得D=107.95kmol/h。
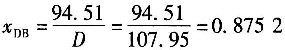
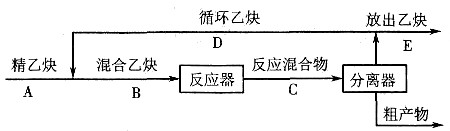
15. 乙烯在银催化剂上用过量空气部分氧化制取环氧乙烷。反应方程如下。
主反应:
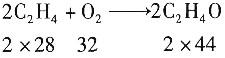
副反应:
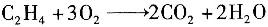
反应器进口混合气体的流量为45000m
3(标准),组成如下表所示。
| 物料组成 |
| 物料组成 | C2H4 | N2 | O2 | 合计 |
| 摩尔分数/% | 3.5 | 82.0 | 14.5 | 100.0 |
乙烯的转化率为32%,反应选择性为69%,则反应器出口气体的流量近似值为______。
- A.57107.5kg
- B.57415.2kg
- C.56981.95kg
- D.11289.9kg
A B C D
B
[解析] 解:取混合气体流量45000m
3为基准。
(1)计算反应器进口气体的平均分子量。
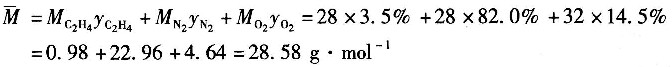
(2)计算反应器进、出口的质量流量。
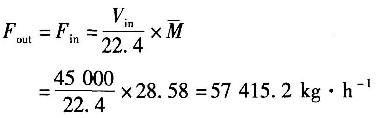
16. 有乙烯和丙烯的气体混合物,摩尔分数分别为80%和20%。已知乙烯和丙烯的C
p,m—T函数式如下。
乙烯:C
p,m1=2.830+28.601×10
-3T-8.726×10
-6T
2(kcal/(kmol·K)
丙烯:C
p,m2=2.253+45.116×10
-3T-13.740×10
-6T
2(kcal/(kmol·K)
则上述混合气体100℃时的定压摩尔热容C
p,m为______。
- A.6.01kJ/(kmol·K)
- B.57.53kJ/(kmol·K)
- C.50.3kJ/(kmol·K)
- D.55.51kJ/(kmol·K)
A B C D
D
[解析] 解:以Cp,m1和Cp,m2分别表示100℃时乙烯和丙烯的理想气体定压摩尔热容。
Cp,m1=2.830+28.601×10-3×373-8.726×10-6×3732=12.3kcal/(kmol·K)
=51.42kJ/(kmol·K)
Cp,m2=2.253+45.116×10-3×373-13.740×10-63732=17.2kcaL/(kmol·K)
=71.87kJ/(kmol·K)
Cp,m=0.8×51.42+0.2×71.87=55.51kJ/(kmol·K)
19. 有一蒸馏塔,输入物料为A、B、C的混合物,进入量为100kg/h,其组成中A占20%,B占30%,塔顶馏出物P中A组分的量为进料中A组分量的98.7%,塔釜液W中A占0.005,B占0.055,C占0.94,求塔顶和塔釜的产量(kg/h)及塔顶馏出物中A的百分数______。
- A.P=48kg,W=52kg,x=41.13%
- B.P=52kg,W=48kg,x=37.96%
- C.P=48kg,W=52kg,x=37.96%
- D.P=48kg,W=52kg,x=2.33%
A B C D
A
[解析] 解:取100kg输入物料为计算基准。
令x=馏出物中A的百分含量,y=馏出物中B的百分含量。
根据题意,已知输入物料中A组分的98.7%自塔顶蒸出,即流股P中A组分的量为
Px=100×20%×98.7%=19.74kg (1)
A组分衡算式:
100×20%=W×0.5%+19.74 (2)
总物料衡算式:
100=P+W (3)
B组分衡算式:
100×30%=W×5.5%+Py (4)
由式(2)得W=52kg,代入式(3)得P=100-52=48kg,代入式(4)得y=56.54%。
由式(1)得
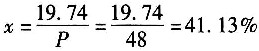
22. 在硫酸生产过程中,二氧化硫催化氧化为三氧化硫。初始气体组成(体积分数)为SO
211%,O
210%,N
279%,氧化过程在570℃,120kPa下进行,转化率为70%。则反应混合物气体中SO
3的分压为______。
- A.9.6kPa
- B.10.01kPa
- C.9.24kPa
- D.53.87kPa
A B C D
A
[解析] 解:SO
2氧化反应方程式为
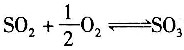
设原料气为100mol。
根据题意,进料气中SO
2为11mol,O
2为10mol,N
2为79mol。
反应后气体
SO
3=11×0.7=7.7mol
SO
2=11-7.7=3.3mol
O
2=10-0.5×11×0.7=6.15mol
N
2=79mol
反应后总摩尔数为96.15mol,其中
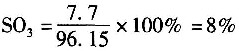
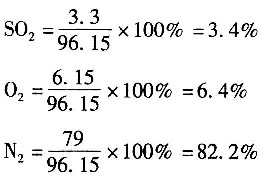
各组分的分压:
p
SO3=0.08×120=9.6kPa
p
SO2=0.034×120=4.08kPa
p
O2=0.064×120=7.68kPa
23. 甲醇脱氢生成甲醛的反应方程式为
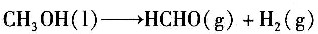
试用燃烧热数据计算0.1013MPa、25℃下的反应热。
25℃下甲醇(1)的燃烧热
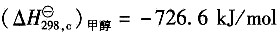
;
25℃下HCHO(g)的燃烧热
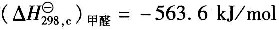
;
25℃下H
2(g)的燃烧热
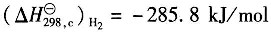
。
- A.-122.8kJ/mol
- B.-1576kJ/mol
- C.122.8kJ/mol
- D.-1290.2kJ/mol
A B C D
C
[解析] 解:0.1013MPa、25℃下的反应热为
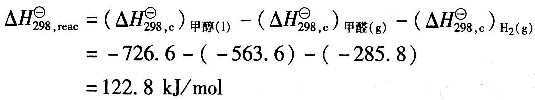
24. 如用98%的硫酸、98%的硝酸和70%的硫酸配制1000kg组成为含硫酸51%、含硝酸44%、含水5%的混合酸配酸过程,已知原料酸及混合酸的微分溶解热分别为:98%的H
2SO
4707.1kJ/kg,98%的HNO
3447.6kJ/kg,70%的H
2SO
4 257.3kJ/kg,混合酸506.26kJ/kg。则酸的配制过程混合热为______。
- A.3.5×105kJ
- B.3.6×104kJ
- C.2.7×104kJ
- D.2.7×105kJ
A B C D
B
[解析] 解:混合热QS=444×707.1+449×447.6+107×257.3-1000×506.26
=3.62×104kJ
二、多选题11. 丙烷充分燃烧时供入空气量为理论量的125%,反应式为C
3H
8+5O
2=3CO
2+4H
2O,每产生1000mol燃烧产物所需的空气摩尔数错误的有______。(已知每mol空气中含O
2 0.21mol,含N
2 0.79mol)
- A.749.2mol
- B.937.0mol
- C.1686.6mol
- D.1324.7mol
A B C D
ACD
[解析] 解:取1mol丙烷为计算基准。
需要氧气:1.25×5=6.25mol;
需要空气:6.25/0.21=29.76mol。
燃烧产物量:O
2 1.25mol,N
2 29.76×0.79=23.51mol,H
2O 4 mol,CO
2 3mol,总计1.25+23.51+4+3=31.76mol。
每1000mol燃烧产物需要的空气量为:
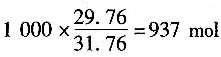
。
16. 已知化学反应n
1A(g)+n
2B(g)→n
3C(g)+n
4D(g)中参与反应的物质在该相态下生成热和燃烧热分别为
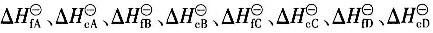
,则该反应的化学反应热计算公式正确的有______。
A.

B.
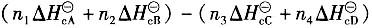
C.
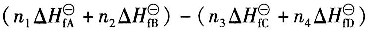
D.
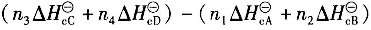
A B C D
 Al2O3的混合物中含杂质44.6%(质量分数,下同),原料硫酸为80%,的H2SO4,其余为H2O。用1100kg Al2O3、2510kg80%的H2SO4,则过量的一种原料的转化率是______。假定Al2O3,全部转化。
Al2O3的混合物中含杂质44.6%(质量分数,下同),原料硫酸为80%,的H2SO4,其余为H2O。用1100kg Al2O3、2510kg80%的H2SO4,则过量的一种原料的转化率是______。假定Al2O3,全部转化。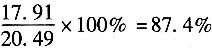 。
。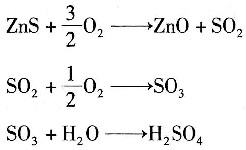
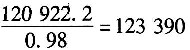 kg 98%的硫酸。
kg 98%的硫酸。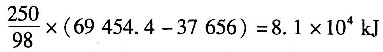
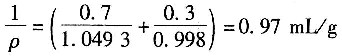

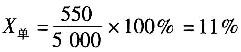
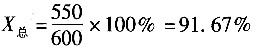
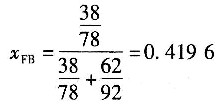
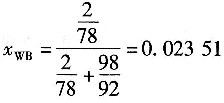
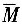 =0.4196×78+(1-0.4196)×92=86.13
=0.4196×78+(1-0.4196)×92=86.13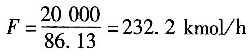

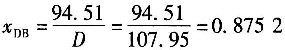
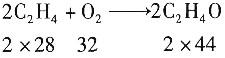

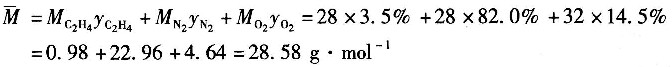
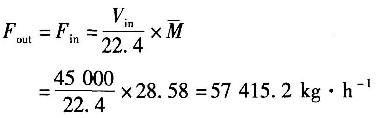
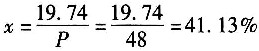
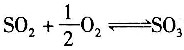
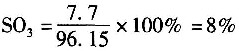
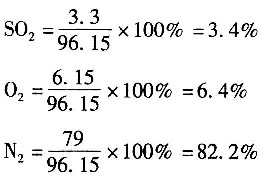
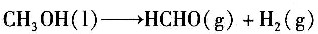 试用燃烧热数据计算0.1013MPa、25℃下的反应热。
试用燃烧热数据计算0.1013MPa、25℃下的反应热。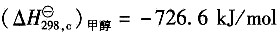 ;
;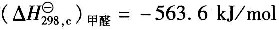 ;
;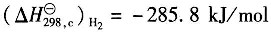 。
。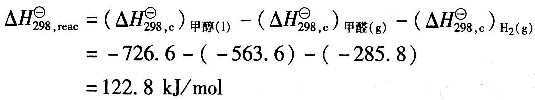
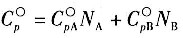
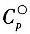 计算
计算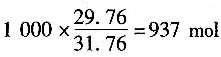 。
。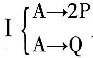 及反应
及反应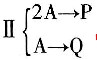 ,已知P为目的产物,P的收率为80%。当P的产量为1kmol时,上述两个反应所需要的A的量不正确的有______。
,已知P为目的产物,P的收率为80%。当P的产量为1kmol时,上述两个反应所需要的A的量不正确的有______。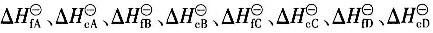 ,则该反应的化学反应热计算公式正确的有______。
,则该反应的化学反应热计算公式正确的有______。